Współczesna onkologia w dużej mierze opiera się na modelu redukcjonistycznym: zidentyfikuj dominującą ścieżkę, precyzyjnie ją namierz i oczekuj regresji guza. Jednak rak wielokrotnie dowiódł, że nie jest chorobą izolowanych ścieżek, lecz adaptacyjnych systemów biologicznych. Guzy nie przegrywają, ponieważ jedna ścieżka jest hamowana – one ewoluują.
Ta świadomość doprowadziła do wzrostu zainteresowania strategiami terapeutycznymi na poziomie systemowym, szczególnie tymi ukierunkowanymi na metabolizm nowotworów. Koncepcja wieloosiowej pułapki metabolicznej stanowi jedno z takich podejść. Zamiast koncentrować się na pojedynczej podatności, wywiera ona skoordynowany nacisk na wiele domen metabolicznych i sygnalizacyjnych, mając na celu wywołanie braku elastyczności metabolicznej – stanu, w którym komórki nowotworowe nie są już w stanie się adaptować.
W tym kontekście większość agentów wywiera presję na określoną oś: metabolizm glukozy, funkcję mitochondriów, mitozę, sygnalizację stresu lub regulację redoks. Jednak żaden agent nie wpisuje się idealnie w ten schemat.
Iwermektyna odgrywa wyjątkową rolę.
Nie jest ona najlepiej rozumiana jako lek o pojedynczym celu, ani nawet jako konwencjonalny środek o działaniu wielocelowym. Iwermektyna działa raczej jako wzmacniacz na poziomie sieci , łącząc i wzmacniając jednocześnie wiele osi pułapki metabolicznej. Ta właściwość może wyjaśniać, dlaczego wykazuje nieproporcjonalnie dużą synergię w połączeniu, pomimo stosunkowo niewielkiej aktywności w monoterapii.
Rak jako system sieciowy i adaptacyjny
Komórki rakowe przeżywają nie dlatego, że są silne, ale dlatego, że mają zdolność adaptacji.
Gdy glikoliza jest zahamowana, guzy zwiększają zależność od fosforylacji oksydacyjnej mitochondriów lub utleniania kwasów tłuszczowych. Gdy funkcja mitochondriów jest upośledzona, powracają one do glikolizy lub aktywują proliferacyjne szlaki ucieczki. Pod wpływem stresu terapeutycznego, uruchamiają programy transkrypcyjne, które przebudowują sieci przetrwania.
Ta zdolność adaptacji jest realizowana za pomocą połączonych ze sobą systemów sygnalizacyjnych, w tym:
-
PI3K/AKT/mTOR → reguluje wzrost, syntezę białek i wykrywanie składników odżywczych
-
Wnt/β-katenina → reguluje łodygowość, plastyczność i oporność
-
YAP/TAZ (szlak Hippo) → integruje sygnały mechaniczne i cytoszkieletowe
-
Układy redoks (ROS, glutation) → kontrolują przeżycie w warunkach stresu oksydacyjnego
-
Mechanizm transportu jądrowego (importyna α/β) → reguluje odpowiedzi transkrypcyjne
Te ścieżki nie działają w izolacji. Tworzą redundantną, odporną sieć , umożliwiającą nowotworom dynamiczną reorganizację pod wpływem presji terapeutycznej.
Kluczowym wyzwaniem nie jest zatem po prostu zahamowanie jednej ścieżki, lecz zakłócenie zdolności sieci do adaptacji .
Wieloosiowa pułapka metaboliczna
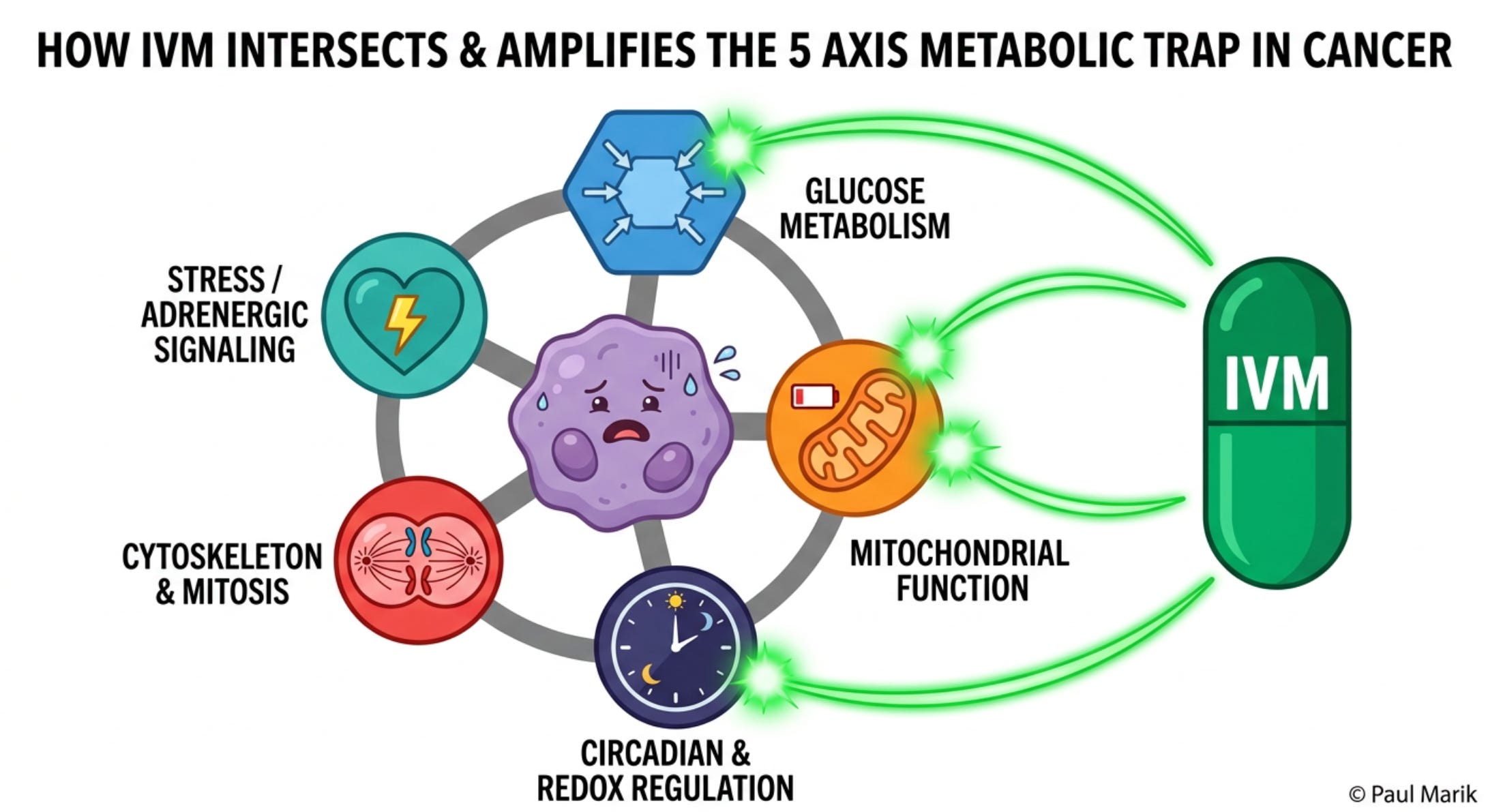
Pułapka metaboliczna rozwiązuje ten problem, oddziałując jednocześnie na pięć głównych osi:
-
Metabolizm glukozy (metformina, berberyna)
-
Funkcja mitochondriów (doksycyklina)
-
Cytoszkielet i mitoza (mebendazol)
-
Sygnalizacja stresu/adrenergiczna (propranolol)
-
Regulacja dobowa i redoks (melatonina)
Każda oś reprezentuje podatność. Jednak guzy mogą kompensować, gdy atakowana jest tylko jedna z nich. Siła pułapki tkwi w koordynacji – blokowaniu wielu dróg ucieczki jednocześnie .
Jednak sama koordynacja nie wystarczy.
Bez integracji terapia wielolekowa grozi przekształceniem się w zbiór równoległych interwencji, a nie w jednolity system. To właśnie tutaj iwermektyna nabiera mechanistycznego znaczenia.
Iwermektyna: integrator osi poprzecznej
Iwermektyna wywiera niezwykle szeroki zakres efektów biologicznych, które krzyżują się z wieloma szlakami istotnymi dla rozwoju raka. Co ważne, nie są to przypadkowe efekty uboczne – zbiegają się one w kluczowych systemach regulacyjnych, które rządzą adaptacją.
1. Hamowanie PI3K/AKT/mTOR (oś sygnalizacji metabolicznej)
Iwermektyna hamuje fosforylację AKT i dalszą sygnalizację mTOR. Ma to kilka konsekwencji:
-
Zmniejsza syntezę białek i wzrost komórek
-
Zaburza wychwyt glukozy i przepływ glikolizy
-
Ogranicza zdolność guza do kompensacji stresu energetycznego
Bezpośrednio wzmacnia to blokadę osi glukozowej wywołaną przez metforminę i berberynę.
2. Supresja Wnt/β-kateniny (oś macierzystości)
Szlak Wnt jest kluczowy dla utrzymania komórek macierzystych raka. Iwermektyna zaburza ten szlak poprzez:
-
Promowanie degradacji β-kateniny
-
Hamowanie transkrypcji genów związanych z macierzystością
-
Zmniejszenie przeżywalności klonogenicznej
Jest to istotne, ponieważ komórki macierzyste nowotworu stanowią źródło oporności i nawrotów .
3. Modulacja YAP/TAZ (sygnalizacja mechaniczna i cytoszkieletowa)
Iwermektyna zakłóca szlak Hippo poprzez hamowanie lokalizacji jądrowej YAP/TAZ.
-
Zmniejsza sygnalizację proliferacyjną
-
Zaburza czucie napięcia cytoszkieletu
-
Zwiększa wrażliwość na środki antymitotyczne
Daje to synergię z substancjami takimi jak mebendazol, które oddziałują na mikrotubule.
4. Hamowanie transportu jądrowego (Importin α/β System)
Jednym z najbardziej unikalnych działań iwermektyny jest hamowanie szlaku importyny α/β.
-
Zapobiega przemieszczaniu się czynników transkrypcyjnych do jądra
-
Osłabia adaptacyjne reakcje ekspresji genów
-
Ogranicza szybkie przeprogramowanie komórkowe
Może to być jeden z najważniejszych – i niedocenianych – mechanizmów.
Komórki nowotworowe przeżywają terapię nie tylko dzięki metabolizmowi, ale także dzięki adaptacji transkrypcyjnej . Iwermektyna bezpośrednio zakłóca ten proces.
5. Dysfunkcja mitochondriów i wytwarzanie ROS
Iwermektyna wywołuje stres mitochondrialny poprzez:
-
Zaburzenie potencjału błony mitochondrialnej
-
Zwiększona produkcja reaktywnych form tlenu (ROS)
-
Zaburzenia fosforylacji oksydacyjnej
Wzmacnia to działanie inhibitorów mitochondrialnych, takich jak doksycyklina.
Jednocześnie zwiększony poziom ROS przybliża komórki do załamania redoks , szczególnie gdy układy antyoksydacyjne są już obciążone.
6. Modulacja kanałów chlorkowych i homeostaza komórkowa
Iwermektyna działa na kanały chlorkowe bramkowane glutaminianem i inne kanały jonowe:
-
Zmienia równowagę jonów wewnątrzkomórkowych
-
Zaburza homeostazę komórkową
-
Może przyczyniać się do sygnalizacji apoptozy
Choć mniej się na to zwraca uwagę, stanowi to dodatkowy poziom destabilizacji komórkowej.
Integracja w sieci
W przeciwieństwie do środków działających głównie na jedną oś, efekty iwermektyny są rozłożone na całą sieć.
W praktyce iwermektyna:
-
Wzmacnia ograniczenie glukozy → poprzez tłumienie sygnału przeżycia AKT/mTOR
-
Wzmacnia stres mitochondrialny → zwiększa ROS i upośledza produkcję energii
-
Wzmacnia zaburzenia cytoszkieletu → poprzez modulację YAP/TAZ
-
Blokuje adaptację transkrypcyjną → poprzez hamowanie transportu jądrowego
-
Zwęża tolerancję redoks → popycha komórki w kierunku niewydolności oksydacyjnej
Iwermektyna nie tworzy zatem nowej osi, lecz łączy już istniejące .
Ograniczanie ucieczki adaptacyjnej
Oporność na leczenie jest w swej istocie wyrazem adaptacyjnej ucieczki.
Wydaje się, że iwermektyna ogranicza ten proces na wielu poziomach:
-
Ucieczka metaboliczna → ograniczenie kompensacji poprzez hamowanie AKT/mTOR
-
Ucieczka od macierzystości → zmniejsza przeżywalność komórek macierzystych raka poprzez supresję Wnt
-
Ucieczka transkrypcyjna → blokuje import adaptacyjnych czynników transkrypcyjnych do jądra
-
Ucieczka redoks → zwiększa stres oksydacyjny poza tolerowane granice
Efekty te zachodzą jednocześnie , co utrudnia komórkom nowotworowym przejście z jednej strategii przetrwania na inną.
Oto istota pułapki metabolicznej:
nie przytłaczająca siła, lecz ograniczenie strategiczne .
Synergia ponad potencjałem
Podstawową zasadą pułapki metabolicznej jest to, że skuteczność nie zależy od maksymalnej siły działania poszczególnych środków, lecz od ich łącznego oddziaływania .
Iwermektyna jest przykładem tej zasady.
W monoterapii wykazuje następujące działanie przeciwnowotworowe:
-
Skromny
-
Zmienny
-
Zależne od kontekstu
Jednakże w połączeniu:
-
Zwiększa zakłócenia szlaków
-
Zwiększa spójność stresu metabolicznego
-
Zmniejsza redundancję w sieci adaptacyjnej
Przekształca to szereg ciśnień parcjalnych w ograniczenie obejmujące cały system .
Jego wartość nie leży w samym tym, co robi, ale w tym, jak zmienia zachowanie systemu .
Od presji do załamania
Komórki nowotworowe mogą wytrzymać znaczny stres, pod warunkiem że zachowają zdolność adaptacji.
Pułapka metaboliczna ma na celu pozbawienie tej elastyczności.
Dzięki iwermektynie działającej jako integrator układ przechodzi z:
-
Odszkodowanie → porażka
-
Adaptacja → nieelastyczność
-
Przetrwanie → załamanie
Celem nie jest natychmiastowa cytotoksyczność, ale postępująca erozja zdolności adaptacyjnych .
Implikacje kliniczne i przyszłe kierunki
Postrzeganie iwermektyny jako wzmacniacza na poziomie sieci ma kilka ważnych implikacji:
1. Racjonalne projektowanie kombinowane
Terapie powinny w pierwszej kolejności obejmować środki oddziałujące na różne szlaki, a nie tylko te, które oddziałują na izolowane mechanizmy.
2. Strategie niskodawkowe i wieloczynnikowe
Zaburzenia na poziomie systemowym można osiągnąć stosując mniejsze dawki wielu środków, co potencjalnie poprawia tolerancję.
3. Rozwój biomarkerów
Przyszłe prace powinny skupić się na markerach:
-
Nieelastyczność metaboliczna
-
Stres oksydacyjny
-
Konwergencja ścieżek
4. Zapobieganie oporności
Zamiast leczyć oporność po jej wystąpieniu, podejścia wielokierunkowe mają na celu zapobieganie ucieczce adaptacyjnej od samego początku .
Ograniczenia i środki ostrożności
Należy podkreślić, że:
-
Większość dowodów na przeciwnowotworowe działanie iwermektyny pozostaje w fazie przedklinicznej
-
Dane kliniczne są ograniczone i niejednorodne
-
Optymalne dawkowanie, harmonogram i kombinacje nie zostały jeszcze określone
Aby wyciągnąć ostateczne wnioski, konieczne jest przeprowadzenie rygorystycznych badań klinicznych.
Wniosek
W pułapce metabolicznej o wielu osiach iwermektyna nie jest po prostu kolejnym lekiem poddanym ponownemu wykorzystaniu.
Jest integratorem systemu .
Łącząc zaburzenia metaboliczne z zakłóceniami sygnału, wzmacniając stres międzyosiowy i ograniczając ucieczkę adaptacyjną, iwermektyna przekształca zbiór interwencji w skoordynowaną strategię terapeutyczną.
Odzwierciedla to szerszą zmianę w onkologii:
Od oddziaływania na pojedyncze ścieżki → do destabilizacji sieci podtrzymujących sam nowotwór.
(tłumaczenie automatyczne Google)